
Tìm hiểu về khí Axetilen (C2H2)
Tìm hiểu về khí Axetilen (C2H2)
18/10/2022
Axetilen C2H2 là một trong những loại khí quen thuộc trong cuộc sống hàng ngày của chúng ta, nó được sử dụng phổ biến trong nhiều lĩnh vực khác nhau. Vậy bạn đã biết khí Axetilen là gì, nó có tính chất và ứng dụng ra sao, địa điểm bán khí Axetilen uy tín, an toàn ở đâu? Hãy cùng Khí công nghiệp Hỷ Vân đi tìm hiểu rõ hơn về loại khí này qua bài viết dưới đây nhé!
1. Khí Axetilen là gì?
Axetilen hay Acetylen có tên trong hệ thống IUPAC là Ethyne. Đây là hợp chất hóa học có công thức là C2H2 với cấu trúc H-C≡C−H. Vì toàn bộ thành phần hóa học chỉ có các nguyên tử hydro và cacbon nên hợp chất này là một hidrocacbon. Đồng thời cũng được coi là ankin đơn giản nhất vì nó chỉ bao gồm hai nguyên tử carbon, được liên kết ba lần với nhau.
Trong thực tế, Axetilen rất không ổn định ở dạng nguyên chất, do đó chúng thường tồn tại ở dạng dung dịch.
Tính chất vật lý
-
- Axetilen là chất khí không màu, không mùi, nhẹ hơn không khí với tỉ trọng 26/29 và ít tan trong nước.
- Axetilen tinh khiết không mùi, nhưng loại thương mại phổ biến trên thị trường thường có mùi giống tỏi do các tạp chất như divinyl sulfide (C4H6S) và phosphine (PH3)
- Đây là chất khí dễ dàng bắt lửa và đốt cháy với ngọn lửa muội. Nguồn lửa có thể bùng phát trở lại nguồn rò rỉ rất dễ dàng. Trong điều kiện tiếp xúc lâu với lửa hoặc nhiệt, các thùng chứa có thể bị vỡ và nổ tung. Do đó Axetilen thường được đựng trong các chai chứa đặc biệt, khác hoàn toàn với các loại khí khác.
Tính chất hóa học
Phản ứng oxy hoá:
C2H2 cháy trong oxi tạo ra CO2 và hơi nước
-
- Phương trình phản ứng: 2C2H2 + 5O2 → 4CO2 + 2H2O
Phản ứng cộng:
C2H2 tham gia phản ứng cộng với chất halogen, hidro halogenuo (HCL, HBr….) Silver nitrate
-
- Phương trình Phản ứng Halogen HC≡CH + Br-Br → Br-CH=CH-Br Br-CH=CH-Br + Br-Br → Br2CH-CHBr2
- Phương trình phản ứng Hidro halogen HC≡CH + HBr → CH2=CHBr
- Phương trình phản ứng với Silver nitrate trong môi trường NH3 HC≡CH + AgNO3 + NH3 + H2O → Ag-C≡C-Ag ↓ màu vàng + NH4NO3
- Phương trình hidrat hoá Khi Axetilen kết hợp với hidrat hoá gây ra phản ứng tạo thành axit axetic (CH3COOH) HC≡CH + H2O (H2SO4) → H-CH=CH-H → CH3COOH
Xem thêm về khí C2H2:
- 8 ứng dụng của khí Axetilen
- Vai trò của khí Acetylene trong hàn cắt hiện đại
- Hàn khí hay hàn gió là gì
2. Các ứng dụng của khí Axetilen.
-
- Axetilen tinh khiết 99,6% hoặc 99,8% chủ yếu được dùng trong các phòng thí nghiệm, trung tâm phân tích, nghiên cứu, bệnh viện.
- Axetilen tinh khiết 99,5% (chứa không quá 0,5% tạp chất) được dùng làm nguyên liệu sản xuất một số chất dẻo polyethene. Khi axetilen bị bán hydro hóa, nó được chuyển thành ethylene (C2H4). Ethylene có thể được sử dụng như một nguyên liệu trong các phản ứng trùng hợp tạo ra polyethene là sản phẩm cuối cùng.
- Axetilen 98% (chứa không quá 2% tạp chất) dùng làm nhiên liệu trong đèn xì oxi-axetilen để hàn hay cắt kim loại. Axetilen bị đốt cháy với oxi tạo ra ngọn lửa rất nóng, có nhiệt độ lên tới hơn 3300 độ C. Năng lượng giải phóng lên tới 11,8 KJ trên mỗi gram nhiên liệu đốt cháy.
- Axetilen còn được dùng để sản xuất axit axetic, rượu etylic…
- Axetilen đã từng được dùng làm nguyên liệu chiếu sáng trong loại đèn axetilen được sử dụng trong các hầm mỏ hoặc các ngọn hải đăng. Canxi cacbua (đất đèn) thường được sử dụng kết hợp với nước để tạo ra axetilen được sử dụng trong đèn. Hiện nay vì tính mất an toàn của nó, hình thức chiếu sáng này đã lỗi thời, không còn được sử dụng và được thay thế bằng điện chiếu sáng và đèn LED.
- Xem thêm: 8 ứng dụng của khí Axetilen

3. Lịch sử phát hiện khí Axetilen
-
- Axetilen được phát hiện lần đầu tiên vào năm 1836, khi Edmund Davy đang thử nghiệm với cacbua kali. Một trong những phản ứng hóa học của ông đã tạo ra một loại khí dễ cháy, hiện nay được gọi là Axetilen. Năm 1859, Marcel Morren đã tạo ra thành công Axetilen khi ông sử dụng các điện cực cacbon để tạo ra hồ quang điện trong môi trường khí hydro. Hồ quang điện xé các nguyên tử cacbon ra khỏi điện cực và liên kết chúng với các nguyên tử hydro để tạo thành phân tử Axetilen. Ông gọi khí này là hydro cacbon hóa.
- Vào cuối những năm 1800, một phương pháp khác đã được phát triển để tạo ra Axetilen bằng cách cho canxi cacbua phản ứng với nước. Điều này tạo ra một dòng khí Axetilen được kiểm soát có thể cháy trong không khí để tạo ra ánh sáng trắng rực rỡ. Đèn lồng cacbua được sử dụng bởi những người thợ mỏ và đèn cacbua được sử dụng để chiếu sáng đường phố trước khi có đèn điện. Năm 1897, Georges Claude và A. Hess phát hiện ra khí Axetilen có thể được bảo quản an toàn bằng cách hòa tan nó trong axeton. Nils Dalen đã sử dụng phương pháp mới này vào năm 1905 để phát triển đèn tín hiệu đường sắt và hải đăng tự động đốt cháy lâu. Năm 1906, Dalen tiếp tục sử dụng Axetilen để hàn và cắt kim loại.
- Vào những năm 1920, công ty BASF của Đức đã phát triển một quy trình sản xuất Axetilen từ khí tự nhiên và hydrocacbon từ dầu mỏ. Nhà máy đầu tiên đi vào hoạt động tại Đức vào năm 1940. Công nghệ này đến Hoa Kỳ vào đầu những năm 1950 và nhanh chóng trở thành phương pháp chính để sản xuất Axetilen.
- Nhu cầu về Axetilen tăng lên khi các quy trình mới được phát triển, để chuyển nó thành chất dẻo và hóa chất hữu ích. Tại Hoa Kỳ, nhu cầu đạt đỉnh vào khoảng thời gian từ năm 1965 đến năm 1970, sau đó giảm mạnh khi xuất hiện các vật liệu thay thế mới, chi phí thấp hơn. Kể từ đầu những năm 1980, nhu cầu về Axetilen đã tăng chậm lại với tốc độ khoảng 2-4% mỗi năm.
- Năm 1991, có tám nhà máy ở Hoa Kỳ sản xuất Axetilen. Họ đã cùng nhau sản xuất tổng cộng 160 triệu kg Axetilen mỗi năm. Trong số này, 66% là từ khí đốt tự nhiên và 15% từ chế biến dầu mỏ. Hầu hết Axetilen từ hai nguồn này đã được sử dụng tại chỗ hoặc gần nơi sản xuất để tạo ra các hóa chất hữu cơ khác. 19% còn lại đến từ canxi cacbua. Một số Axetilen từ nguồn này được sử dụng để sản xuất hóa chất hữu cơ, và phần còn lại được các nhà sản xuất khí công nghiệp sử dụng để nạp vào các bình điều áp cho các khách hàng hàn và cắt kim loại tại địa phương.
- Ở Tây Âu, khí đốt tự nhiên và dầu mỏ là nguồn nguyên liệu chính của Axetilen, trong khi cacbua canxi là nguồn chính ở Đông Âu và Nhật Bản.
4. Tạo ra Axetilen trong phòng thí nghiệm
Quá trình đơn giản nhất là phản ứng canxi cacbua (đất đèn) với nước để tạo ra khí Axetilen cùng với một dạng bùn canxi cacbonat, được gọi là vôi ngậm nước. Cho vài mẩu nhỏ canxi cacbua vào ống nghiệm đã đựng sẵn 1ml nước, hoặc ngược lại cho nước nhỏ từ từ vào 1 lượng canxi cacbua, sau đó đậy nhanh lại bằng nút có ống dẫn khí và đầu vuốt nhọn. Đốt khí sinh ra ở đầu ống vuốt nhọn, khí axetilen sẽ được tạo ra từ đầu ống vuốt nhọn. Phản ứng hóa học có thể được viết dưới dạng: CaC2 + 2H2O → C2H2 + Ca(OH)2 . Với cách điều chế này khí axetilen tạo ra không được tinh khiết do hàm lượng canxi cacbua chứa nhiều tạp chất (H2S, NH3, PH3)
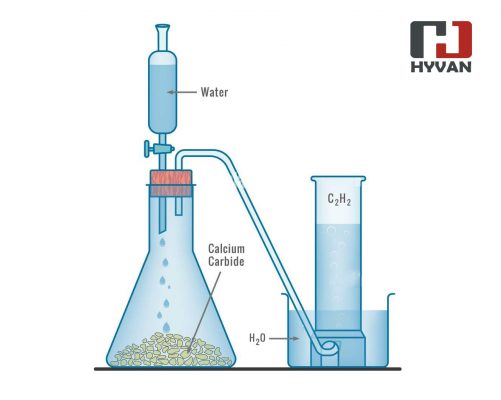
Hoặc cũng có thể điều chế axetilen bằng cách cho cacbon tác dụng với hidro khi có hồ quang điện: 2C + H2 → C2H2
5. Quy trình sản xuất Axetilen công nghiệp
Đối với mục đích thương mại, Axetilen có thể được sản xuất từ một số nguyên liệu thô khác nhau tùy thuộc vào quá trình sử dụng. Các quy trình khác sử dụng khí tự nhiên, chủ yếu là mêtan, hoặc hydrocacbon từ dầu mỏ như dầu thô, naphtha, hoặc dầu boongke C làm nguyên liệu. Than cũng có thể được sử dụng. Các quá trình này sử dụng nhiệt độ cao để chuyển đổi nguyên liệu thô thành nhiều loại khí khác nhau, bao gồm hydro, carbon monoxide, carbon dioxide, acetylene và các loại khí khác. Phương trình phản ứng chuyển hóa metan thành axetilen và hiđro: 2CH4 + 15000°C → C2H2 + 3H2 . Các khí khác là sản phẩm của quá trình đốt cháy với oxy. Để tách Axetilen, nó được hòa tan trong dung môi như nước, amoniac khan, metanol làm lạnh, hoặc axeton, hoặc một số dung môi khác tùy thuộc vào quá trình.
Có hai quá trình chuyển đổi cơ bản được sử dụng để tạo ra Axetilen. Một là một quá trình phản ứng hóa học, xảy ra ở nhiệt độ bình thường. Quá trình còn lại là cracking nhiệt, xảy ra ở nhiệt độ cực cao. Dưới đây là các chuỗi hoạt động điển hình được sử dụng để chuyển đổi các nguyên liệu thô khác nhau thành Axetilen theo từng quy trình cơ bản.
a. Quá trình phản ứng hóa học
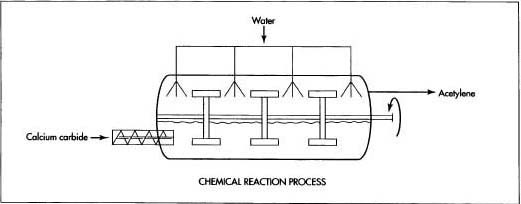
Axetilen có thể được tạo ra bởi phản ứng hóa học giữa canxi cacbua và nước. Phản ứng này tạo ra một lượng nhiệt đáng kể, nhiệt lượng này phải được loại bỏ để tránh khí Axetilen phát nổ. Có một số biến thể của quá trình này, trong đó canxi cacbua được thêm vào nước hoặc ngược lại. Cả hai biến thể này được gọi là quá trình ướt vì một lượng nước dư thừa được sử dụng để hấp thụ nhiệt của phản ứng. Một biến thể thứ ba, được gọi là quá trình khô, chỉ sử dụng một lượng nước hạn chế, sau đó sẽ bốc hơi khi hấp thụ nhiệt. Biến thể đầu tiên được sử dụng phổ biến nhất và được mô tả như sau:
-
- Hầu hết các nhà máy tạo Axetilen công suất lớn sử dụng một băng tải trục vít quay để cấp các hạt cacbua canxi (đất đèn) vào buồng phản ứng, đã được làm đầy nước đến một mức nhất định. Các hạt có kích thước khoảng 2×6 mm, đây là kích thước bề mặt tiếp xúc phù hợp để cho phép phản ứng xảy ra hoàn toàn. Tốc độ cấp nguyên liệu được xác định bởi tốc độ dòng khí mong muốn tạo ra, và được điều khiển bởi một công tắc áp suất trong buồng. Nếu quá nhiều khí được tạo ra cùng một lúc, công tắc áp suất sẽ mở và cắt giảm tốc độ nạp.
- Để đảm bảo phản ứng xảy ra hoàn toàn, dung dịch chứa các hạt canxi cacbua và nước được khuấy liên tục bằng một bộ cánh khuấy quay bên trong buồng phản ứng. Điều này cũng ngăn chặn bất kỳ hạt nào nổi trên bề mặt, nơi chúng có thể quá nhiệt và bốc cháy.
- Khí Axetilen nổi bọt lên bề mặt và được hút ra dưới áp suất thấp. Khi nó rời khỏi buồng phản ứng, khí được làm mát bằng một tia nước. Đây cũng là lượng nước bổ sung vào buồng phản ứng để giữ cho phản ứng tiếp tục khi canxi cacbua mới được thêm vào. Sau khi khí được làm lạnh, nó đi qua một bộ chống chớp từ thiết bị ở phía dưới của buồng, ngăn chặn bất kỳ sự đánh lửa ngẫu nhiên nào.
- Khi canxi cacbua phản ứng với nước, nó tạo thành một dạng bùn canxi cacbonat chìm xuống đáy của khoang. Phản ứng cần phải được dừng lại định kỳ để loại bỏ lượng bùn tích tụ. Bùn sau khi thoát ra khỏi khoang và được bơm vào một ao chứa, nơi canxi cacbonat lắng xuống và nước được rút ra ngoài. Canxi cacbonat đậm đặc sau đó được làm khô và bán để sử dụng như một chất xử lý nước thải công nghiệp, chất trung hòa axit hoặc chất điều hòa đất cho xây dựng đường.
b. Quá trình nứt nhiệt (cracking nhiệt)
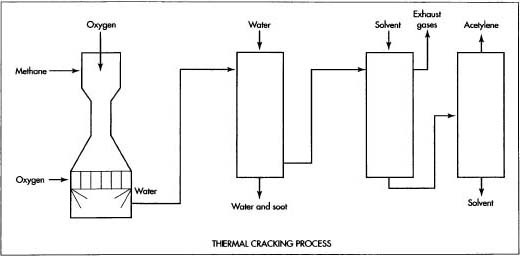
Axetilen cũng có thể được tạo từ quá trình cracking nhiệt, đây là phương pháp tăng nhiệt độ của các hydrocacbon khác nhau đến mức mà các liên kết nguyên tử của chúng bị đứt hoặc nứt. Sau khi các nguyên tử hydrocacbon tách rời nhau, chúng có thể được tái tạo lại để tạo thành các vật liệu mới. Quá trình này được sử dụng rộng rãi để chuyển đổi dầu hoặc khí tự nhiên thành nhiều loại hóa chất. Có một số biến thể của quá trình này tùy thuộc vào nguyên liệu thô được sử dụng và phương pháp tăng nhiệt độ. Một số quy trình cracking sử dụng hồ quang điện để đốt nóng nguyên liệu, trong khi những quy trình khác sử dụng buồng đốt, đốt cháy một phần hydrocacbon để tạo ra ngọn lửa. Một lượng Axetilen được tạo ra như một sản phẩm phụ của quá trình cracking hơi nước, được sử dụng để sản xuất ethylen (C2H4). Quy trình phổ biến nhất là sử dụng buồng đốt để làm nóng và đốt cháy khí tự nhiên như mô tả dưới đây:
-
- Khí tự nhiên, chủ yếu là mêtan (CH4), được làm nóng đến khoảng 650°C. Việc làm nóng khí trước sẽ khiến nó tự bốc cháy khi đến đầu đốt và cần ít oxy hơn để đốt cháy.
- Khí được làm nóng đi qua một đường ống hẹp, tại đây oxy được bơm vào và trộn với khí nóng.
- Hỗn hợp khí nóng và oxy đi qua một bộ khuếch tán, bộ khuếch tán làm chậm vận tốc của nó đến tốc độ mong muốn. Đây là điều rất quan trọng, nếu vận tốc quá cao, khí đi vào sẽ thổi tắt ngọn lửa trong đầu đốt. Nếu vận tốc quá thấp, ngọn lửa có thể bùng phát trở lại và đốt cháy khí trước khi nó đến đầu đốt.
- Hỗn hợp khí chảy vào buồng đốt gồm hơn 100 kênh hẹp. Khi khí chảy vào mỗi kênh, nó tự bốc cháy và tạo ra ngọn lửa làm tăng nhiệt độ khí lên khoảng 1.500°C. Một lượng nhỏ oxy được thêm vào trong đầu đốt để ổn định quá trình đốt cháy.
- Khí đốt chảy vào không gian phản ứng ngay bên ngoài đầu đốt, nơi nhiệt độ cao làm cho khoảng một phần ba khí metan chuyển hóa thành Axetilen, 2 phần khí metan còn lại bị đốt cháy. Toàn bộ quá trình đốt cháy chỉ diễn ra trong vài mili giây.
- Khí cháy nhanh chóng được dập tắt bằng các vòi phun nước tại điểm mà sự chuyển hóa thành Axetilen là lớn nhất. Khí được làm mát chứa một lượng lớn carbon monoxide và hydro, và một lượng nhỏ muội than carbon, cùng với carbon dioxide, Axetilen, mêtan và các khí khác.
- Khí đi qua máy lọc nước để loại bỏ muội than. Sau đó, tiếp tục đi qua một máy lọc thứ hai, nơi nó được phun với một dung môi được gọi là N-metylpyrolidinone để hấp thụ Axetilen.
- Dung môi được bơm vào tháp tách, tại đó Axetilen được đun sôi để tách ra khỏi dung môi và được rút ra ở đỉnh tháp dưới dạng khí, trong khi dung môi được rút ra khỏi đáy tháp.
6. Lưu ý trong bảo quản và xử lý
-
- Bởi vì Axetilen rất dễ phát nổ, nó cần phải được bảo quản và xử lý hết sức cẩn thận. Khi nó được vận chuyển qua đường ống, áp suất được giữ rất thấp và chiều dài của đường ống cũng rất ngắn.
- Axetilen an toàn với con người nếu tiếp xúc với một lượng nhỏ hơn 2,5% trong thời gian dưới 1 giờ đồng hồ. Nếu vượt quá nồng độ cho phép, con người sẽ cảm thấy buồn nôn, nhức đầu, khó thở, đau tức ngực, da tái xanh hoặc hôn mê. Nếu tiếp xúc trực tiếp qua da sẽ có hiện tượng phát ban.
- Trong các hoạt động sản xuất hàng ngày, khí axetilen được nén vào các bình chứa để cung cấp cho các cơ sở hàn cắt kim loại. Chúng phải sử dụng các bình chứa đặc biệt, các bình chứa hình trụ được làm đầy bằng vật liệu hấp thụ, như đất tảo cát và một lượng nhỏ axeton. Axetilen được bơm vào các bình ở áp suất khoảng 2.070 kPa, tại đây nó được hòa tan trong axeton. Sau khi hòa tan, nó sẽ mất khả năng nổ, giúp vận chuyển an toàn. Khi van bình khí được mở, sự giảm áp suất làm cho một lượng Axetilen hóa hơi trở lại thành khí và chảy qua ống nối tới mỏ hàn hoặc mỏ cắt.
- Hạn chế hư hại vật lý các bình chứa axetilen. Bảo quản ở những khu vực riêng, tách riêng với các chất khác, tránh các nguồn bắt cháy, nhiệt, lửa, điện.
- Bảo quản nơi khô ráo, thoáng mát. Yêu cầu có rào chắn che đậy, bảng hiệu cảnh báo cẩn thận.
7. Địa chỉ bán khí Axetilen uy tín, chất lượng.
Với những tính chất, ứng dụng phổ biến của mình, axetilen được điều chế và bán rộng rãi trên thị trường. Khí công nghiệp Hỷ Vân là một trong những đơn vị cung cấp khí Axetilen uy tín, an toàn. Quý khách vui lòng liên hệ số điện thoại 0969.690.155 để được tư vấn trực tiếp, miễn phí!
Link nội dung: https://unie.edu.vn/trong-cac-chat-sau-chat-nao-la-axetilen-a66826.html